د زينب عبدالبديع تكتب: المقاومة البكتيرية للمضادات واستراتيجيات التصدي للمضادات الحيوية

باحث -المعمل المرجعي للرقابة على الإنتاج الداجني – معهد بحوث الصحة الحيوانية – مركز البحوث الزراعية- مصر
مقاومة المضادات الحيوية (Antimicrobial resistance, or AMR), هي قدرة البكتيريا على مقاومة تأثير المضادات الحيوية والنجاة منها، مما يجعل علاج العدوى البكتيرية أكثر صعوبة وتعقيدا.
وتُعد مقاومة المضادات الحيوية واحدة من أبرز التحديات الصحية على مستوى العالم التي تواجه الصحة العامة في القرن الحادي والعشرين. ورغم تعدد المضادات الحيوية الطبيعية والاصطناعية التي أُضيفت إلى ساحة المعركة،
إلا أن البكتيريا تكتشف دائمًا استراتيجيات مضادة لتقليل فعالية المضادات الحيوية. وذلك تزامنا مع الاستخدام المفرط وغير المنظم للمضادات الحيوية في الطب البشري والبيطري والزراعة،
وقد ظهرت سلالات بكتيرية قادرة على النجاة من تأثير هذه الأدوية، مما أدى إلى زيادة معدلات الوفيات، إطالة فترة العلاج، وارتفاع التكاليف الطبية. حيث يُتوقع أن تتسبب في وفاة 10 ملايين شخص سنويًا بحلول عام 2050 إذا لم يتم اتخاذ إجراءات فعّالة لمواجهة هذه الأزمة.
تعمل المضادات الحيوية بشكل انتقائي ضد أهداف محددة وعمليات أيضية خاصة بالبكتيريا. وفي مواجهة تأثير المضادات الحيوية من قبل البكتيريا اكتشف الباحثون آليات مقاومة جديدة للمضادات الحيوية في البكتيريا، تشمل دخولها في حالة سكون، وإفراز بروتينات تحمي هدفها، وتنظيم عملية الأيض، وتفعيل أنظمة الإصلاح الذاتي، والتي تشكل مجتمعةً نظام الدفاع البكتيري ضد المضادات الحيوية.
وفي هذا المقال، سنستعرض أسباب والطرق والآليات الرئيسية للمقاومة في البكتيريا
الأسباب الرئيسية لظهور مقاومة المضادات الحيوية AMR:
- الاستخدام المفرط وغير المنضبط للمضادات الحيوية في الطب البشري: تناول المضادات الحيوية دون استشارة الطبيب، خاصة للأمراض الفيروسية (كالزكام والإنفلونزا) التي لا تستجيب لها.
- نقص السيطرة على العدوى في المستشفيات والمرافق الطبية، مما يسهل انتقال البكتيريا المقاومة بين المرضى والطاقم الطبي
- الاستعمال المكثف في الزراعة لتعزيز نمو النباتات وحماية المحاصيل.
- الاستخدام في الطب البيطري لعلاج الحيوانات أو الوقاية من الأمراض واستخدام المضادات الحيوية كإضافات اعلاف و دافع نمو للحيوانات او الطيور .
- وجود ثغرات في أنظمة الرقابة والإشراف على المضادات الحيوية.
- ضعف الوعي عند الافراد خاصة في الدول النامية مثل التوقف عن تناول الدواء قبل انتهاء المدة العلاجية الموصوفة، مما يترك البكتيريا الأضعف لتنمو وتتكاثر.
آليات المقاومة الرئيسية
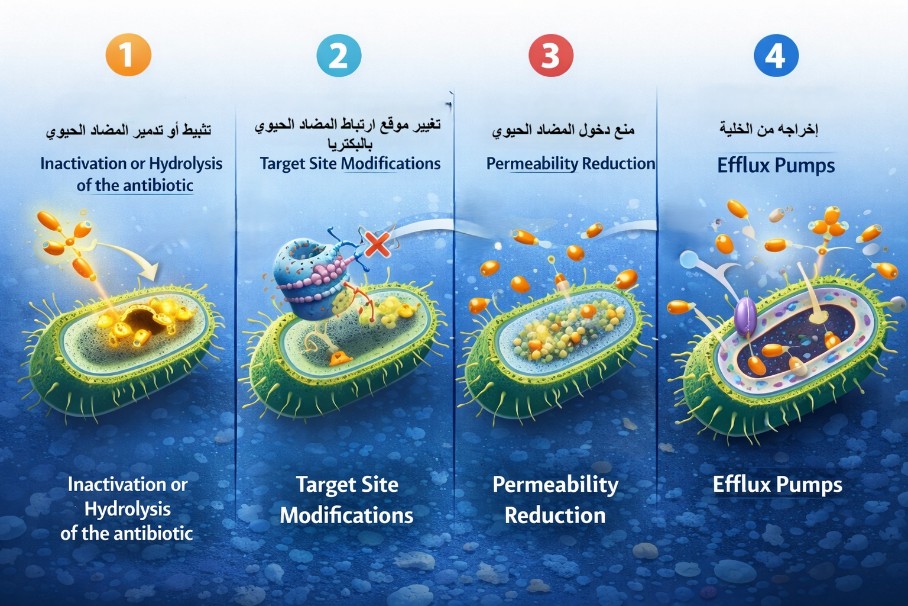
البكتيريا تطور عدة استراتيجيات وآليات للبقاء على قيد الحياة أمام هذه المضادات الحيوية ، والتي يمكن تصنيفها إلى أربع فئات رئيسية:
- تثبيط أو تدمير المضاد الحيوي (Inactivation or Hydrolysis of the antibiotic)
- تغيير موقع ارتباط المضاد الحيوي بالبكتريا ((Target Site Modifications
- منع دخول المضاد الحيوي (Permeability Reduction)
- (Efflux Pumps)
هذه الآليات غالباً ما تكون تعتمد على الطفرات الجينية والنقل الأفقي للجينات عبر البلازميدات (plasmids) أو الترانسبوزونات(transposons) كوسيلتين أساسيتين للبقاء أمام المضادات الحيوية. مما يسمح بانتشارها بسرعة بين الأنواع البكتيرية.
- تثبيط أو تدمير المضاد الحيويInactivation or Hydrolysis of the antibiotic
بعض البكتيريا تنتج إنزيمات تدمر جزيئات المضاد الحيوي قبل أن تصل إلى هدفها داخل الخلية، مثل بيتا لاكتاماز (β-lactamase,)، وإنزيمات تعطيل الأمينوغليكوزيدات (aminoglycoside inactivating enzymes)، وكلورامفينيكول أسيتيل ترانسفيراز(chloramphenicol acetyltransferase).
اهم هذه الانزيمات هو إنزيم بيتا-لاكتاماز (Beta-Lactamase) يعمل على قطع حلقة البيتا لاكتام في المضاد الحيوي البنسلين مما يؤدي إلى تحلله قبل وصوله هدفه داخل الخلية البكتيرية. هذا الإنزيم ينتج بواسطة جينات مثل (blaTEM) غالبًا ما تكون مشفَّرة على بلازميدات أو عناصر متنقلة في بكتيريا، مما يسهل انتقالها بين البكتيريا. و هناك دراسة نشرت في مجلة Nature Reviews Microbiology (2018) تظهر كيف ينتشر هذا الجين عالمياً، مما يجعل المضادات مثل الأموكسيسيلين غير فعالة.
تُعد هذه الألية من أهم أسباب انتشار المقاومة المتعددة للأدوية (MDR) في مسببات الأمراض مثل:
- الإشريكية القولونية ( coli) التي تعيش في الأمعاء بشكل طبيعي، لكن سلالات معينة يمكن أن تسبب عدوى خطيرة خارج الجهاز الهضمي، مثل عدوى المسالك البولية والتهاب السحايا
- الكلبسيلة الرئوية (Klebsiella pneumoniae) التي يمكن أن تسبب التهاب رئوي، عدوى بولية، خراج الكبد، وتجرثم الدم
- الزائفة الزنجارية (Pseudomonas aerugino) التي تتواجد في البيئات الرطبة، وتُفضل المناطق الرطبة كالمستشفيات والمراحيض و قد يسبب عدوى خارجية بسيطة إلى أمراض مهددة للحياة، خاصة لدى المرضى ذوي المناعة المنخفضة.
- تغيير موقع ارتباط المضاد الحيوي بالبكتريا (Target Site Modifications)
يتطلب تأثير المضادات الحيوية المضاد للبكتيريا ارتباطها بالموقع المستهدف في البكتريا، حيث أن أي طفرة أو تعديل في هذا الموقع يعوق هذا الارتباط الطبيعي، مما يؤثر على فعالية المضادات الحيوية.
لذلك تقوم بعض البكتيريا بتغيير شكل أو تركيب الجزيء الحيوي (البروتينات المستهدفة) الذي يرتبط به المضادات الحيوية داخلها، مما يقلل من فعالية الدواء. وذلك عن طريق تغييرات في البروتينات المستهدفة من المضادات الحيوية داخل البكتريا. وقد أصبحت هذه البروتينات المعدلة من قبل البكتريا منتشرة بين العديد من الأنواع البكتيرية الآن.
من أمثلة هذا:
- تعديل الريبوسومات(ribosomes) في حالة مقاومة الأمينوغليكوزيدات(aminoglycosides)، أو تغيير بروتينات الارتباط الخاصة بالبنسلين (PBPs) في حالة مقاومة المكورات العنقودية الذهبية (Staphylococcus aureus) للبنسلين والميثيسيلين وهذه البكتريا شائعة تتواجد بشكل طبيعي على جلد الإنسان وفي الأنف، تتجمع على شكل عناقيد عنب. يمكن أن تكون غير ضارة، لكنها قد تسبب عدوى خطيرة (مثل التهابات الجلد، الالتهاب الرئوي، والتهاب صمامات القلب) خاصة إذا دخلت الجسم، وتزداد خطورتها عندما تطور مقاومة للمضادات الحيوية.
- ايضا تكونت مقاومة التتراسيكلين(tetracycline) نتيجة بروتينات المقاومة Tet(M) و Tet(O)، حيث تتفاعل هذه البروتينات مع الريبوسومات (ribosomes) وتزيح المضاد الحيوي التتراسيكلين (tetracycline)
والتي تم التعرف عليها لأول مرة في أنواع البكتيريا العقدية (Streptococcus)التي تسبب أمراضاً مختلفة مثل التهاب الحلق، والتهاب اللوزتين، وتسوس الأسنان، والتهاب الرئة، والتهاب السحايا.
والعطيفة الصائمية (Campylobacter jejuni) هي نوع شائع من البكتيريا الحلزونية التي تسبب التهابات معوية وأحد الأسباب الرئيسية للإسهال المعدي المنقول عبر الطعام، خاصة من الدواجن والحليب غير المبستر والمياه الملوثة
هذه الآليات لا تُعطّل المضاد الحيوي نفسه، بل تمنع وصوله إلى هدفه أو تقلل ارتباطه به, وتُعد من الأسباب الرئيسية لفشل العلاج في حالات مثل السل المقاوم للمضاد الحيوي الريفامبين.
يصعب كشفها مخبريًا مقارنة بآليات مثل إنتاج بيتا-لاكتاماز، وتحتاج إلى تقنيات جزيئية متقدمة.
- منع دخول المضاد الحيوي او انخفاض نفاذية الغشاء (Decreased Membrane Permeability)
تقليل النفاذية (Permeability Reduction) هو إحدى آليات مقاومة البكتيريا للمضادات الحيوية، حيث تمنع البكتيريا دخول الدواء إلى داخلها عبر تعديل بنيتها الخارجية أو تقليل عدد القنوات الناقلة.
بعض البكتيريا، خاصة سالبة الجرام، تمتلك غشاء خارجي (جدار خلوي) يعمل كحاجز يمنع دخول المواد الضارة. تقوم البكتيريا عند مقاومة المضادات الحيوية بـتغيّر تركيب جدارها الخلوي أو قنواتها البروتينية لتقليل دخول الدواء، مما يقلل من اختراق المضادات الخلية إلى داخل الخلية البكتيرية. وذلك عن طريق:
- تقليل عدد أو نوعية القنوات البروتينية (Porins) التي تسمح بمرور المضاد الحيوي.
- تعديل تركيب الغشاء الخارجي ليصبح أقل نفاذية.
- زيادة سماكة الجدار أو تغيير شحنته لتقليل التفاعل مع الدواء.
- Pseudomonas aeruginosa تُعرف بالعربية باسم (الزائفة الزنجارية)، وهي بكتيريا قادرة على التسبب في عدوى خطيرة، خاصةً لدى الأشخاص ذوي المناعة المنخفضة وشائعه في المستشفيات، وتتسبب بالعدوى المكتسبة من المستشفيات (Hospital-acquired infections). ، وتشتهر بمقاومتها المتعددة للمضادات الحيوية بسبب تقليل نفاذية الغشاء الخارجي ، وتصيب أجزاء مختلفة من الجسم مثل الجلد والرئة والمجرى الدموي، وتسبب حالات كـ “أذن السباح” (التهاب الأذن الخارجية).عدوى في الجلد والجروح و تسمم الدم (Bacteremia) والتهابات الجهاز التنفسي وعدوى المسالك البولية ويتم العلاج بالمضادات الحيوية، لكن المقاومة تجعل علاجها صعبًا
- مضخات الطرد (Efflux Pumps)
- وواسعة الانتشار للدفاع الخلوي، وهي عاملٌ رئيسيٌ في مقاومة الأدوية المتعددة (MDR) في البكتيريا والفطريات والخلايا السرطانية. مضخات الطرد هي بروتينات ناقلة مُدمجة في غشاء الخلية للكائن الحي (البكتيريا، الفطريات، الخلايا البشرية، إلخ).
- تتمثل وظيفتها الأساسية في النقل النشط للمواد السامة، بما في ذلك المضادات الحيوية، والعوامل الكيميائية، والأصباغ، والمنظفات، وغيرها من المركبات السامة، من داخل الخلية (السيتوبلازم/الحيز المحيط بالخلية) إلى البيئة الخارجية.
- ومن خلال طرد هذه المركبات بنشاط، فإنها تخفض تركيز الدواء داخل الخلية إلى مستويات دون السامة، مما يمنع الدواء من الوصول إلى هدفه داخل الخلية وبالتالي يمنع ويمنع تأثيره. وهي موجودة في كل مكان تقريبًا: توجد في جميع الكائنات الحية تقريبًا، مما يشير إلى دور فسيولوجي قديم وأساسي (مثل تنظيم مستويات المغذيات/المعادن الثقيلة، وطرد الفضلات الأيضية، أو جزيئات الدفاع المضيف).
- تُعتبر مضخات الطرد من أكثرو أسرع الآليات شيوعاً وأكثرها فعالية، التي تُسهم في كلٍ من المقاومة الذاتية (الطبيعية) والمكتسبة (المتطورة) للأدوية، وخاصةً المقاومة المتعددة للأدوية. هذه الآلية مسؤولة عن مقاومة أدوية مثل التتراسيكلين(tetracyclines) والماكروليدات(macrolides)،
- وتُعد من أسباب فشل العلاج في حالات العدوى المزمنة,و ذلك لوجود العديد من أنظمة الإخراج النشطة غير المتخصصة، مما يؤدي إلى مقاومة متعددة للأدوية و يجعل البكتيريا قادرة على النجاة حتى عند استخدام تركيزات عالية من المضاد الحيوي
- تشير العديد من الدراسات على سبيل المثال، تقارير منظمة الصحة العالمية (WHO) عن مقاومة مضادات الميكروبات إلى أن مضخات التدفق الخارجي تمثل 20-50% من حالات مقاومة المضادات الحيوية البكتيرية
- نظرا لدورها المحوري في مقاومة المضادات الحيوية المتعددة، تُعتبر مضخات الإخراج أهدافًا علاجية رئيسية. ولذلك يركّز الباحثون على استهدافها باستخدام مثبطات مضخات الإخراج (EPIs) ،وهي مركبات مصممة لحجب نشاط هذه المضخات، مما يزيد من التركيز الفعال للمضاد الحيوي داخل الخلايا ويعيد فعالية الدواء.
- إنتاج بيوفيلم :
البيوفيلم هو مجتمع معقد من الكائنات الدقيقة (مثل البكتيريا، الفطريات، أو الطفيليات) ملتصقة بسطح ما، تغمر نفسها بمصفوفة خارجية متعددة الطبقات تتكون من مواد بوليمرية خارجية (EPS) مثل سكريات(polysaccharides)، البروتينات، والحمض النووي الخارجي(extrinsic DNA). هذه المصفوفة تحمي الخلايا من البيئة الخارجية و يعمل كدرع واقٍ للبكتيريا، مما يجعل البيوفيلم مقاومًا للمضادات الحيوية والدفاعات المناعية. إنتاج البيوفيلم عملية متعددة المراحل، وهي شائعة في البيئات الطبيعية والطبية، مثل الأجهزة الطبية أو الأسطح داخل الجسم.
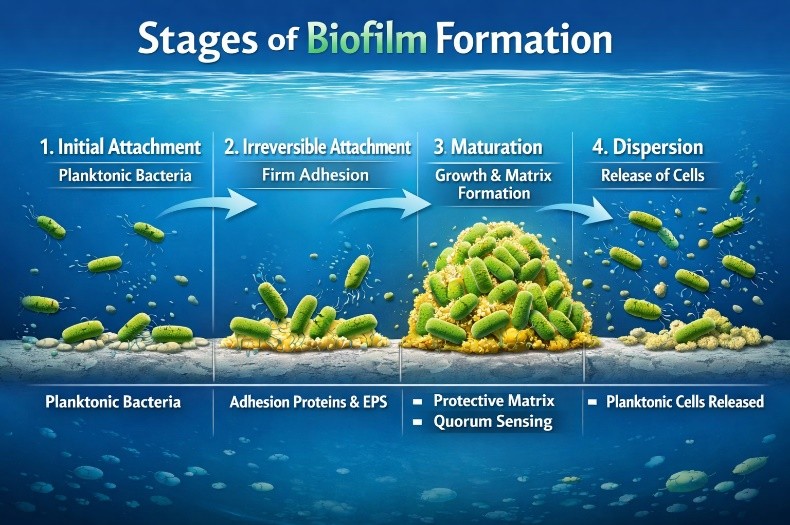
مراحل تكوين البيوفيلم:
- الالتصاق الأولي (Initial Attachment)
تبدأ الخلايا الميكروبية العائمة والحرّة (الخلايا البلانكتونية) بالاقتراب من سطح ما، ثم يتم الالتصاق عبر قوى فيزيائية ضعيفة او الأعضاء الحركية للبكتيريا، مثل الأسواط (Flagella) والأهداب (Pili). في هذه المرحلة، يمكن إزالة الخلايا بسهولة.
- الالتصاق غير العكسي وإنتاج المواد خارج الخلية (Irreversible Attachment & EPS Production)
تتثبت الخلايا على السطح بشكل دائم وتبدأ البكتيريا بإفراز مواد لاصقه لزجة (Slime) التي تتكون أساسًا من المواد البوليمرية خارج الخلية (EPS تستخدم البكتيريا جزيئات التصاق الخلوية المتخصصة لتثبيت نفسها بقوة.
المواد البوليمرية (EPS) هذه المصفوفة المعقدة تتكون بشكل أساسي من عديد السكريات خارج الخلية (Extracellular Polysaccharides): وهي المكون الهيكلي الرئيسي الذي يوفر الدعم والقوةوالبروتينات ولحمض النووي خارج الخلية(eDNA). توفر الـ EPS الحماية ضد العوامل الخارجية مثل المضادات الحيوية والاستجابة المناعية للحيوان المضيف.
- التطور المبكر وتكوين المستعمرات الدقيقة (Early Development & Microcolony Formation)
تتكاثر الخلايا الملتصقة وتتجمع، مشكلةً طبقات متعددة وهياكل على شكل أبراج أو فطر تُعرف باسم المستعمرات الدقيقة (Microcolonies) يزيد تكاثر الخلايا وإفراز الـ EPS، وتبدأ الخلايا في التعبير عن جينات معينة مرتبطة بالبيوفيلم . تلعب إشارات استشعار النصاب (Quorum Sensing)و هي آ لية تواصل جماعي بين البكتيريا ، دورًا حيويًا في تنظيم نمو البيوفيلم وتكوين بنيته، حيث تتواصل الخلايا فيما بينها حول كثافتها الخلوية عبر إفراز واستقبال جزيئات إشارية تُسمى(autoinducer) وعندما يصل تركيز هذه الجزيئات إلى حد معين، تبدأ البكتيريا في تفعيل جينات جماعية تشمل مقاومة المضادات الحيوية.
- النضج (Maturation)
يصل البيوفيلم إلى أقصى حجم وتعقيد له، ويكتسب بنية ثلاثية الأبعاد (3D) متطورة مع قنوات مائية. تستمر الخلايا في النمو والانقسام داخل مصفوفة EPS السميكة. تساعد القنوات المائية على نقل العناصر الغذائية والأكسجين إلى الخلايا العميقة وإزالة الفضلات، مما يضمن بقاء المجتمع. ويصبح البيوفيلم في هذه المرحلة سميكًا ومقاومًا جدًا للمضادات الحيوية والمطهرات.
- التشتت والانتشار (Dispersion or Detachment)
تنفصل بعض الخلايا عن البيوفيلم الناضج وتعود إلى حالتها البلانكتونية الحرة. وتحدث هذه المرحلة استجابةً لنقص المغذيات أو تراكم الفضلات أو بسبب إشارات جينية محددة. تنفصل الخلايا بشكل فردي أو ككتل صغيرة، وتبحث عن أسطح جديدة للالتصاق بها وتكوين بيوفيلم جديد.
دور البيوفيلم في مقاومة المضادات الحيوية يعيق اختراق المضادات الحيوية ويوفر بيئة منخفضة النمو، مما يجعل الخلايا داخله أكثر مقاومة للمضادات بنسبة تصل إلى 1000 مرة مقارنةً بالخلايا البلانكتونية.
يرتبط البيوفيلم ايضا بالعديد من الالتهابات المزمنة (مثل عدوى القسطرات الطبية مثل القسطرات الوريدية والمفاصل الصناعية، وتسوس الأسنان).
يمثل البيوفيلم تحديًا كبيرًا في البيئات الصناعية، إذ يؤدي إلى تآكلًا (Corrosion) في الأنابيب وأغشية الترشيح وتلوثًا في أنظمة المياه و انسداد أغشية الترشيح المستخدمة في أنظمة معالجة المياه وتلوث شبكات المياه، مما يؤثر على جودة المياه وسلامتها .
الخلاصة
إن فهم طرق وآليات مقاومة المضادات الحيوية في البكتيريا يُعد خطوة أساسية نحو تطوير استراتيجيات فعالة لمكافحة هذه الظاهرة. يتطلب الأمر تعاوناً دولياً للحد من الاستخدام المفرط للمضادات الحيوية، وتعزيز البحث العلمي لإيجاد حلول مبتكرة. كما أن نشر الوعي بين الأطباء والمرضى حول الاستخدام الرشيد للمضادات الحيوية يُعد من أهم الخطوات للحد من انتشار المقاومة.